- En primer lugar, veremos qué es la espectrometría.
- Después, estudiaremos la espectroscopía de masa y veremos algunos ejemplos para entenderla mejor.
- Luego aprenderemos sobre la espectroscopía de absorción atómica y la espectroscopía de Raman.
- Para terminar, analizaremos la espectroscopía infrarroja y la ultravioleta visible.
¿Qué es la espectroscopía?
Antes de empezar, veamos qué es la espectroscopía:
La espectroscopía es una técnica mediante la que podemos medir cuánta luz absorbe, refleja o emite un objeto o una disolución.
La espectroscopía sirve para comprender las características de una sustancia química, a partir del análisis de la cantidad de luz que absorbe. Esto nos ayuda a determinar cuáles son los componentes de una sustancia.
Tenemos varios tipos de espectroscopía, en función de para qué la utilizamos. En este artículo, nos centraremos en los siguientes:
- Espectroscopía de masas.
- Espectroscopía de absorción atómica.
- Espectroscopía Raman.
- Espectroscopía infrarroja.
- Espectroscopía ultravioleta visible.
Espectroscopía de masas
La espectroscopía de masas (o espectroscopía atómica de masas) es un método empleado para determinar la masa atómica de los átomos o moléculas de una muestra, mediante la ionización de una especie química y la clasificación de los iones, en función de su relación, masa o carga.
La mayoría de los espectrómetros de masas usan una técnica denominada ionización por impacto de electrones. Esta técnica utiliza un haz de electrones para eliminar un electrón (o electrones) de una molécula, lo que forma un catión radical. Este catión radical también se denomina ion padre o ion molecular.
Un catión radical, ion padre o ion molecular tiene una carga positiva y un electrón no compartido:
$$M + e^{-}\rightarrow M^{+\cdot}+2e^{^{-}}$$
Es decir:
$$molecula + electron\ de\ alta\ energia \rightarrow ion\ molecular + 2\ electrones$$
Veamos un ejemplo para entender esto mejor:
Consideremos la molécula de metano (CH4). Esta molécula formará un catión radical, según la ecuación anterior, de la siguiente manera:
Supongamos que tenemos una muestra de metano (CH4). En primer lugar, se introduce la muestra de gas en el espectrómetro. A continuación, se emiten electrones sobre las moléculas de gas, que pueden romperse en fragmentos y crear cationes radicales. Estas partículas cargadas se dirigen a un detector de iones, tras ser desviadas por un fuerte campo magnético que divide los iones en función de su relación masa-carga (m/z).
Al aumentar el campo magnético, los iones de los isótopos más pesados se desplazan hacia el detector de iones. Este detector de iones está conectado a un ordenador, que indica el espectro de masas de la muestra. El detector de iones puede identificar su relación masa-carga (que es su masa atómica), y el número de átomos que llegan al detector para cada valor m/z.
También, es importante que conozcamos el concepto de espectro de masas, antes de ver un gráfico que ejemplifica lo que acabamos de estudiar:
Se denomina espectro de masas a un gráfico que muestra la intensidad de la señal del detector frente a la masa atómica del ion.
Veamos el caso del espectro de masas del cobre (Cu).
Este espectro de masas nos muestra la existencia de dos isótopos de cobre. En concreto, nos indica las abundancias fraccionarias de ambos isótopos. Así, observando el espectro de masas, podemos saber que el cobre elemental tiene un 69,17 % de 63Cu y un 30,83 % de 65Cu.
Los isótopos son átomos del mismo elemento con el mismo número de protones (número atómico) pero con diferente número de masa (diferente número de neutrones).
 Fig. 1: Espectro de masas del cobre (Cu).
Fig. 1: Espectro de masas del cobre (Cu).
Podemos observar la intensidad relativa de dos isótopos del cobre, en concreto el 63Cu y el 65Cu.
En el gráfico del espectro de masas, m/z también puede escribirse como masa atómica por carga o relación masa-carga.
Si todavía te confunde este tema, ¡no te estreses! Dentro de un rato veremos más ejemplos relacionados con los gráficos del espectro de masas.
Basándote en tus conocimientos sobre la espectrometría de masas, ¿cuál de las siguientes afirmaciones es cierta?
a) Los datos obtenidos de la espectrometría de masas nos indican los estados de oxidación comunes de los elementos.
b) La espectrometría de masas muestra las tendencias del tamaño atómico dentro de la tabla periódica.
c) La espectrometría de masas apoya la existencia de isótopos.
La respuesta correcta es la opción C: La espectroscopía de masas se utiliza para determinar la masa de los átomos individuales de un elemento.
Ecuación de la espectroscopía de masas
La espectrometría de masas explica la relación entre el espectro de masas de un elemento y las masas de los isótopos de ese elemento. Recuerda que los elementos se presentan en la naturaleza como mezclas de isótopos.
Podemos utilizar la información de la espectroscopía de masas para calcular la masa atómica relativa de un elemento, utilizando la siguiente ecuación:
$$A_{r}=\frac{\sum (masa\ del\ isotopo\cdot abundancia\ del\ isotopo)}{100}$$
Veamos un ejemplo, para practicar:
Tenemos el espectro de masas del neón. Observa que muestra tres picos, o tres isótopos del neón: 20Ne (90,9 % de abundancia), 21Ne (0,3 % de abundancia) y 22Ne (8,8 % de abundancia).
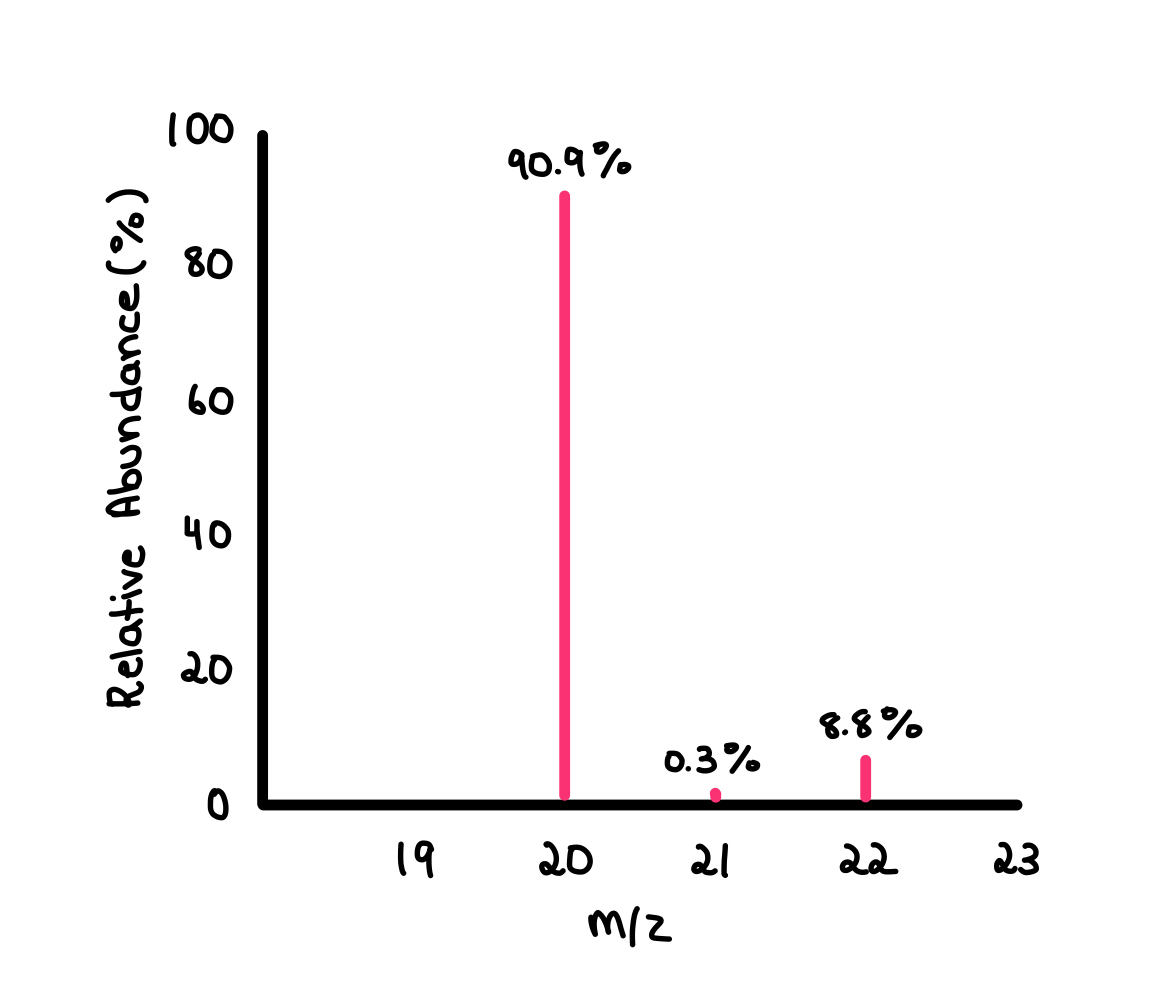
Fig. 2: Espectro de masas del neón (Ne).
Podemos utilizar la ecuación anterior para averiguar la masa atómica relativa del Neón:
$$A_{r}=\frac{\sum (masa\ del\ isotopo\cdot abundancia\ del\ isotopo)}{100}$$
$$A_{r}=\frac{\sum (20\cdot 90.9)+(21\cdot 0.3)+(22\cdot 8.8)}{100}=20.2$$
¿Sabías que la espectrometría de masas también puede emplearse para identificar compuestos orgánicos en química orgánica? Durante el proceso de espectrometría de masas, la muestra es bombardeada con electrones de alta energía, lo que provoca la fragmentación del compuesto. En este caso, el espectro de masas es un poco diferente: el ion molecular provoca el pico de mayor relación m/z. Este pico se conoce como pico padre y nos indica la masa molecular relativa de la muestra.
Veamos un ejemplo de esto; en concreto, con la propanona (CH3COCH3):
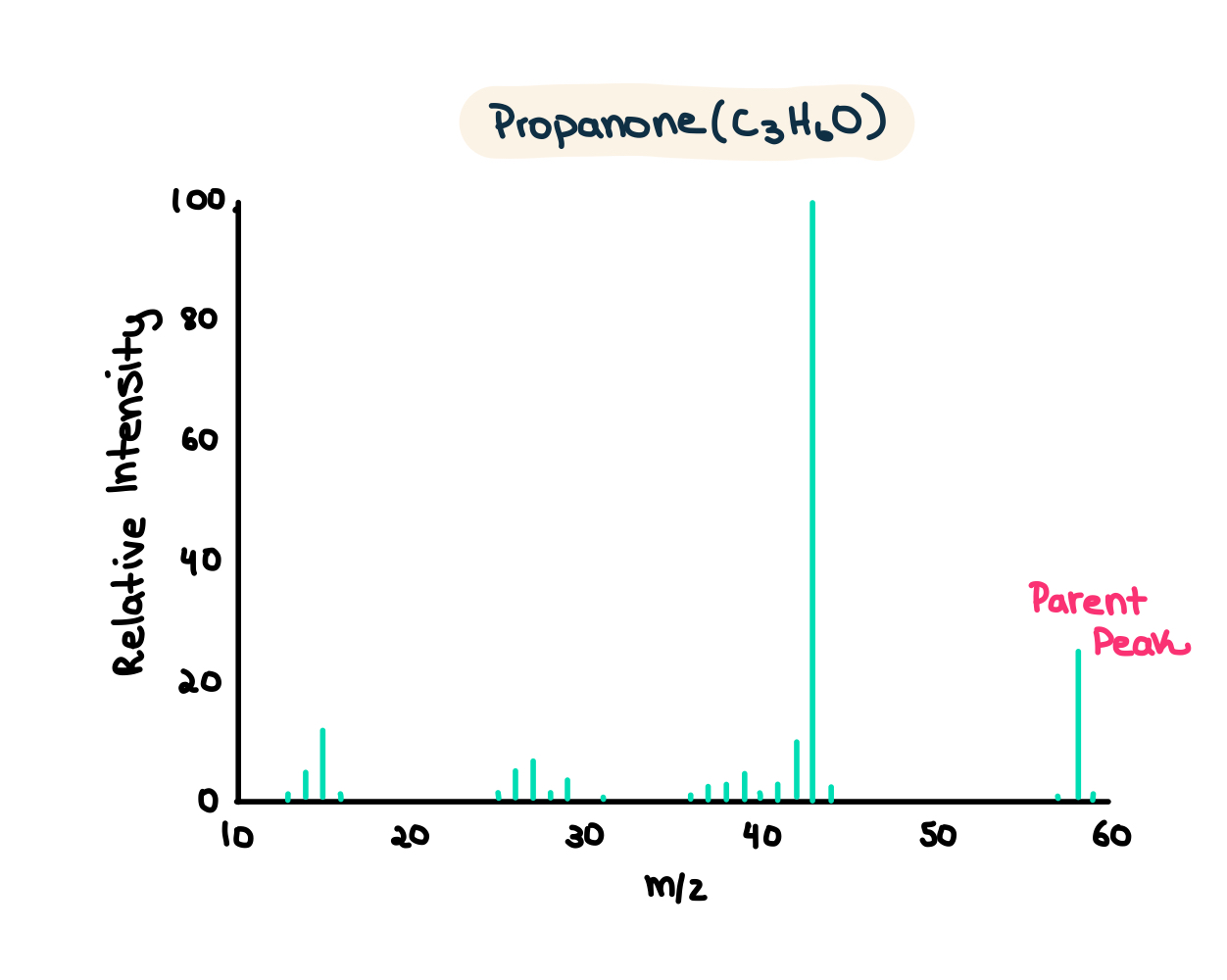
Fig. 3: El espectro de masas de la propanona (CH3COCH3) tiene un pico padre con una relación masa/carga de 58.
Gráficos y elementos
Veamos los gráficos (espectros de masas) de algunos elementos:
El flúor (F) y el yodo (I) solo tienen un pico en su espectro de masas. Así, tanto el 19F como el 127I tienen una abundancia del 100 %. Por otro lado, el bromo elemental presenta dos picos, por lo que tiene un 51 % de bromo-79 y un 49 % de bromo-81. El cloro también tiene dos picos en su espectro de masas: 76 % 35Cl, y 24 % 37Cl.
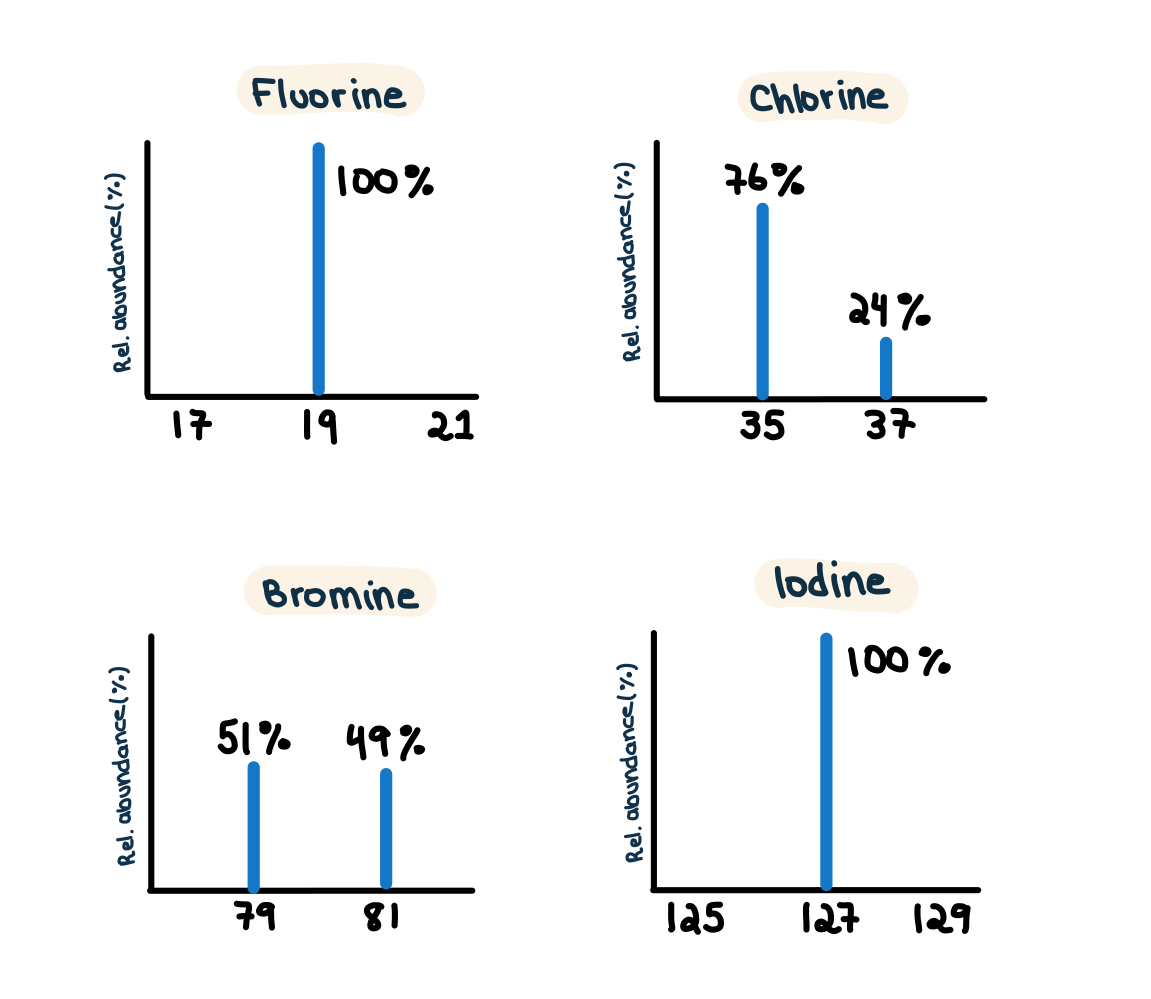
Fig. 4: Espectros de masas de algunos elementos: flúor (F), cloro (Cl), bromo (Br) y yodo (I).
A continuación, veamos el espectro de masas del selenio. ¿Puedes adivinar cuántos isótopos de selenio (Se) existen? Si has dicho 5, ¡tienes razón!
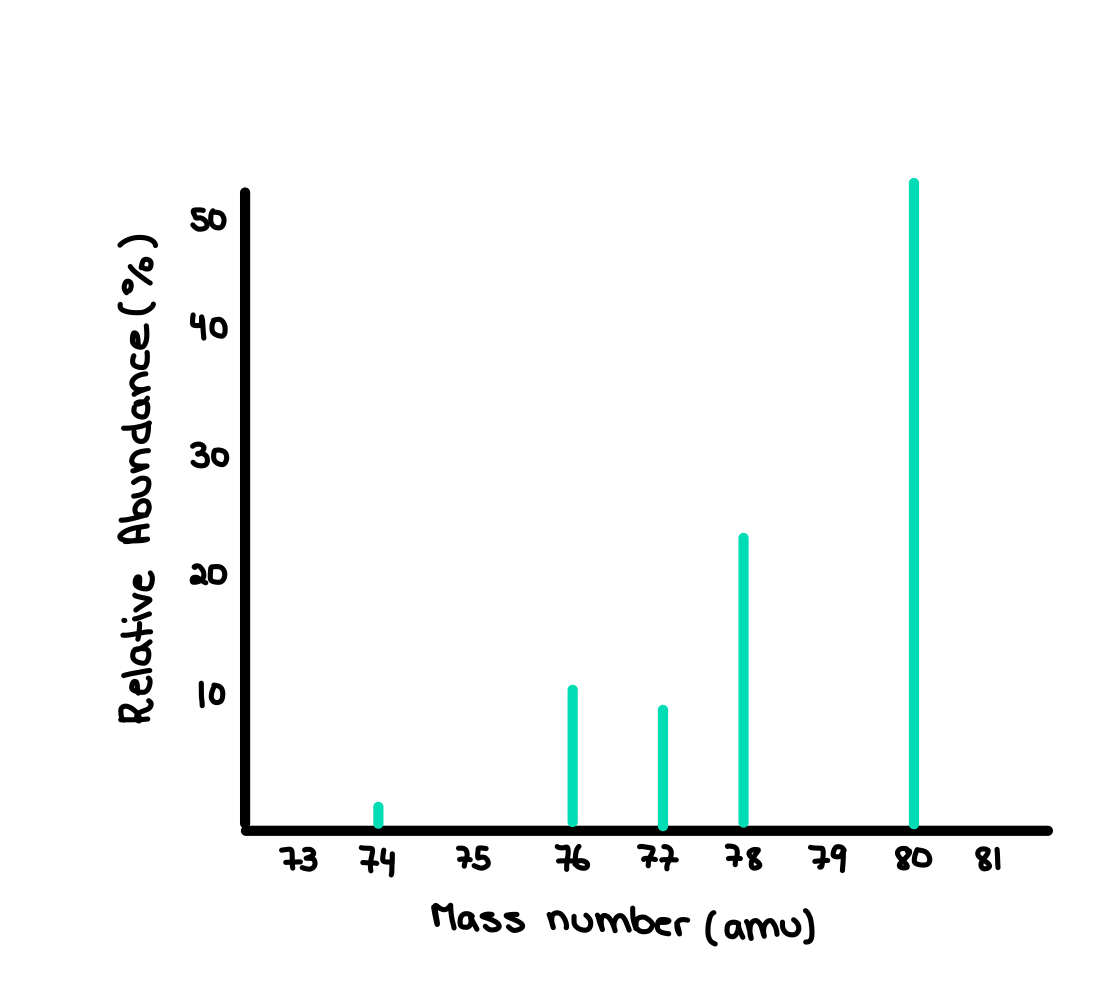
Fig. 5: Espectro de masas del selenio (Se).
Espectroscopía de absorción atómica
Pasemos a ver otro tipo de espectroscopía: la espectroscopía de absorción atómica.
La espectroscopía de absorción atómica es un proceso mediante el cual se analizan los espectros de luz visible o ultravioleta, para determinar de manera cuantitativa la luz química emitida por los átomos gaseosos.
Este es un proceso que se utiliza en la química para saber cuál es la concentración del analito, que es un elemento concreto de la muestra.
Funcionamiento de la espectroscopía de absorción atómica
Veamos ahora cómo funciona la espectroscopía de absorción atómica. Esta técnica está basada en la ley de Beer-Lambert, que se relaciona con la absorción de luz por parte de los elementos y lo relaciona con las propiedades que tiene el elemento concreto. Los electrones pueden trasladarse a niveles de energía más alta gracias a que absorben energía. Esta, a su vez, se corresponde con una luz que tiene una longitud de onda concreta; gracias a ella, podemos saber cuál es el elemento que se encuentra en la muestra, ya que cada longitud de onda se corresponde con el elemento concreto.
Espectroscopía Raman
Otro tipo de espectroscopía es la Raman.
La espectroscopía Raman es un tipo de espectroscopía que se usa para analizar espectros de frecuencia baja, entre los que se encuentran, por ejemplo, los vibratorios.
Este tipo de espectroscopía recibe este nombre porque fue descubierta por el físico Chandrasekhara Venkata Raman en 1928, que recibió el Premio Nobel en 1930 gracias a esto.Se basa en la dispersión inelástica de la luz formada por un solo color (monocromática). Es muy eficiente para descubrir cuál es la composición química y la estructura molecular de una sustancia.
Funcionamiento de la espectroscopía Raman
En primer lugar, lo que tenemos que hacer es que la luz interaccione con la sustancia (ya sea líquida, sólida o gaseosa), para que se produzca una dispersión elástica de los fotones (o dispersión de Rayleigh), que consiste en la dispersión de la luz de una radiación electromagnética. Esta dispersión es producida por ciertas partículas que tienen un tamaño menor al de los fotones que están siendo dispersados. Algunos de estos fotones dispersados (1/10000000 aproximadamente) lo hacen en una frecuencia distinta, lo que se conoce como efecto Raman o dispersión inelástica.
Como curiosidad, la dispersión elástica de los fotones, o dispersión de Rayleigh, es la responsable de que veamos el cielo azul.
Espectroscopía infrarroja
¿Quieres saber más sobre otro tipo de espectroscopía? Pues, pasemos a la espectroscopía infrarroja.
La espectroscopia infrarroja, o de infrarrojos, es una técnica analítica utilizada para identificar los grupos funcionales de las moléculas orgánicas.
Hay dos tipos de espectrómetros utilizados en la espectroscopia de infrarrojos: el espectrómetro de radiación infrarroja dispersiva y el espectrómetro de radiación infrarroja por transformación de Fourier.
En el proceso de la espectroscopía de infrarrojos tienen lugar los siguientes pasos:
- Se hace pasar un haz de radiación a través de una muestra.
- La muestra, que se encuentra en un espectrómetro, absorbe la radiación infrarroja.
- Una vez detectadas y analizadas las absorciones, el espectro de absorción se imprime o se muestra en un ordenador.
Un espectro de absorción es un gráfico que muestra cómo una sustancia química absorbe la radiación en un rango de frecuencias.
Espectroscopía infrarroja de compuestos orgánicos
Todos los compuestos orgánicos absorben la radiación infrarroja, por medio de los enlaces entre las moléculas, a diferentes longitudes de onda.
Vibración de compuestos orgánicos
Cuando los átomos se encuentran en pares, vibran constantemente. Cuando las moléculas orgánicas absorben la radiación infrarroja, los enlaces entre los distintos átomos vibran aún más. Debido a ello, los enlaces covalentes de la molécula también vibran y se ven obligados a estirarse, doblarse o retorcerse. Todas las moléculas vibran a una frecuencia específica. Cada enlace dentro de una molécula tiene una frecuencia de vibración natural única.
El grado de vibración depende de tres factores principales:
- La fuerza del enlace: los enlaces más fuertes vibran a una frecuencia más alta.
- La masa del átomo: los átomos más pesados vibran a una frecuencia más baja.
- La longitud del enlace.
Identificación de moléculas orgánicas
Un espectro infrarrojo de una molécula es un gráfico que se produce una vez realizado el proceso de espectroscopia infrarroja. Veamos un ejemplo a continuación:

Fig. 6: Ejemplo del espectro infrarrojo de una molécula.
En el espectro de infrarrojos, la transmitancia se representa en el eje y, mientras que el número de onda se representa en el eje X. Como podemos ver, el espectro consiste en una serie de caídas en la transmitancia, a ciertas longitudes de onda, que (confusamente) se llaman picos o bandas. Estos picos o bandas representan las vibraciones causadas cuando se absorbe la radiación infrarroja.
- La transmitancia mide el porcentaje de radiación que atraviesa una muestra.
- El número de onda es la cantidad de ondas a una distancia determinada. Esta distancia, a su vez, se conoce como longitud de onda. El número de onda es \(\frac {1}{longitud\ de\ onda}\), por lo que son inversamente proporcionales. Esta medida se utiliza para la frecuencia.
Esta información puede permitirnos identificar grupos funcionales en la molécula. La tabla de datos de la espectroscopia de infrarrojos, tal y como se muestra arriba, se emplea para relacionar los diferentes picos del espectro con los grupos funcionales que podrían haberlos provocado. Los grupos funcionales de la molécula se encuentran en la región entre 4000 cm-1 y 1500 cm-1 del espectro infrarrojo.
Región de huella dactilar de la espectroscopía infrarroja
La región de la huella dactilar es la zona del espectro que está por debajo de 1500 cm-1. Esta región contiene absorciones para algunas vibraciones complicadas, que suelen estar causadas por la flexión o el estiramiento de enlaces simples. Por ello, el patrón en esta región es muy complicado y único para la molécula.
Existe una base de datos en la que se han registrado los espectros infrarrojos de moléculas orgánicas conocidas. Por lo tanto, los espectros infrarrojos producidos para un compuesto complejo desconocido pueden compararse con la base de datos.

Fig. 7: Espectro que destaca la posición de la región de la huella dactilar y la región del grupo funcional.
Ventajas y desventajas de la espectroscopía infrarroja
Como todas las técnicas, la espectroscopia de infrarrojos puede resultar muy útil, pero también tiene sus trampas.
Ventajas
- Las muestras que se visualizan no requieren ninguna preparación especial, como la introducción de un colorante radiactivo en ellas.
- Tiene una alta velocidad de exploración. Toda la información necesaria para toda la gama de frecuencias puede obtenerse en cuestión de segundos.
- El espectrómetro de infrarrojos tiene una resolución muy alta.
- Tiene una amplia gama de aplicaciones, tanto en el análisis cualitativo como en el cuantitativo, por lo que puede utilizarse para analizar casi todos los compuestos orgánicos.
Desventajas
- Si una muestra contiene agua, la espectroscopia de infrarrojos no es aplicable: un disolvente como el agua absorbería la radiación infrarroja.
- A veces, puede haber complicaciones: no podemos aclarar completamente la estructura de un compuesto basándonos en un único espectro de radiación infrarroja.
- La espectroscopia de infrarrojos puede limitarse a ciertas condiciones para el análisis cuantitativo (donde se requieren números y no solo categorías, como “enlace N-H”).
Espectroscopía ultravioleta visible
Veamos una definición de la espectroscopía ultravioleta visible:
La espectroscopía ultravioleta visible es un tipo de espectroscopía en la que se emiten fotones. Se usa radiación ultravioleta y visible (con una longitud de onda entre 380 nm y 780 nm); con esto se consigue que los electrones pasen de un orbital a otro y que las emisiones se puedan medir.
Se puede utilizar para determinar cuáles son los grupos funcionales que forman moléculas, qué elementos se encuentran en una mezcla y para conocer la concentración de una muestra coloreada.
Espectroscopía - Enseñanzas más importantes
- La espectroscopía es una técnica mediante la que podemos medir cuánta luz absorbe, refleja o emite un objeto o una disolución.
- Sirve para analizar las características de una sustancia química, a partir del análisis de la cantidad de luz que absorbe. Esto nos ayuda a determinar los componentes de una sustancia.
- Hay diferentes tipos de espectroscopía, según las técnicas que se lleven a cabo y para qué se utilicen.
- La espectroscopía de masas (o espectroscopía atómica de masas) es un método utilizado para determinar la masa atómica de los átomos o moléculas de una muestra, mediante la ionización de una especie química y la clasificación de los iones, en función de su relación masa-carga.
- La espectroscopía de absorción atómica es un proceso mediante el cual se analizan los espectros, para determinar de manera cuantitativa la luz química emitida por los átomos gaseosos.
- La espectroscopía Raman es un tipo de espectroscopía que se emplea para analizar espectros de frecuencia baja, entre los que se encuentran, por ejemplo, los vibratorios. Se basa en la dispersión inelástica de la luz formada por un solo color (monocromática). Es muy eficiente para descubrir la composición química y la estructura molecular de una sustancia.
- La espectroscopia infrarroja, o de infrarrojos, es una técnica analítica usada para identificar los grupos funcionales de las moléculas orgánicas.
Temas similares en Química
Temas relacionados Átomos y moléculas
¿Cómo te aseguras de que tu contenido sea preciso y confiable?
En StudySmarter, has creado una plataforma de aprendizaje que atiende a millones de estudiantes. Conoce a las personas que trabajan arduamente para ofrecer contenido basado en hechos y garantizar que esté verificado.
Proceso de creación de contenido:
Lily Hulatt es una especialista en contenido digital con más de tres años de experiencia en estrategia de contenido y diseño curricular. Obtuvo su doctorado en Literatura Inglesa en la Universidad de Durham en 2022, enseñó en el Departamento de Estudios Ingleses de la Universidad de Durham y ha contribuido a varias publicaciones. Lily se especializa en Literatura Inglesa, Lengua Inglesa, Historia y Filosofía.
Conoce a Lily
Control de calidad del contenido:
Gabriel Freitas es un ingeniero en inteligencia artificial con una sólida experiencia en desarrollo de software, algoritmos de aprendizaje automático e IA generativa, incluidas aplicaciones de grandes modelos de lenguaje (LLM). Graduado en Ingeniería Eléctrica de la Universidad de São Paulo, actualmente cursa una maestría en Ingeniería Informática en la Universidad de Campinas, especializándose en temas de aprendizaje automático. Gabriel tiene una sólida formación en ingeniería de software y ha trabajado en proyectos que involucran visión por computadora, IA integrada y aplicaciones LLM.
Conoce a Gabriel Gabriel














