- La velocidad de la reacción hacia delante y la velocidad de la reacción hacia atrás son iguales.
- Las concentraciones de los productos y de las reacciones siguen siendo las mismas.
Pero, ¿y si quieres conocer la composición de esta mezcla de equilibrio? Si intentas medir las cantidades de productos o reactivos en la disolución, es probable que acabes perturbando el sistema. En su lugar, podemos utilizar la constante de equilibrio. En este artículo, vamos a centrarnos específicamente en la constante de equilibrio Kc.
La constante de equilibrio es un valor que relaciona las cantidades de reactivos y productos en una reacción reversible en equilibrio.
¡Continúa leyendo para aprender más sobre la constante de equilibrio Kc!
- Este artículo trata sobre la constante de equilibrio, Kc.
- Empezaremos explicando qué es Kc y repasaremos la fórmula empleada para calcularla.
- Después veremos cómo se calculan las unidades de Kc y trabajaremos juntos en dos ejemplos.
- A continuación, repasaremos algunas preguntas de examen para que puedas practicar el cálculo de Kc.
- Después, veremos qué puedes deducir de la magnitud de Kc.
- Por último, abordaremos qué factores afectan al valor de Kc.
¿Cuál es la constante de equilibrio Kc?
Como hemos dicho antes, la constante de equilibrio es un valor que relaciona las cantidades de reactivos y productos de una mezcla en equilibrio. Hay algunos tipos diferentes de constante de equilibrio, pero hoy nos centraremos en Kc.
Kc es una constante de equilibrio que relaciona la concentración de reactivos y la concentración de productos en una reacción reversible en equilibrio.
Hay que tener en cuenta dos cosas cuando se trata de la constante de equilibrio Kc:
- Cuanto mayor sea el valor de Kc, mayor será la proporción de producto respecto al reactivo en el equilibrio.
- El valor de Kc para una reacción concreta a una temperatura determinada es siempre el mismo, independientemente de la cantidad de productos o reactantes con la que empieces.
Fórmula para calcular Kc
Tomemos una reacción de equilibrio general, que se muestra a continuación.
$$aA_{(aq)}+bB_{(aq)}\rightleftharpoons cC_{(aq)}+dD_{(aq)}$$
Kc mide la concentración. Esto significa que nuestros productos y reactantes deben ser líquidos, acuosos o gaseosos. Para empezar, estudiaremos los equilibrios dinámicos homogéneos, que son sistemas en los que todos los reactantes y productos se encuentran en el mismo estado. Más adelante veremos los equilibrios heterogéneos.
En esta reacción, los reactivos A y B reaccionan para formar los productos C y D en la relación molar a:b:c:d.
Por supuesto, como se trata de una reacción reversible, podrías mirarlo desde el otro lado: C y D reaccionan para formar A y B. Sin embargo, solo lo miraremos desde una dirección para no complicar más las cosas.
¿Cuál es la ecuación de Kc? Pues es así:
$$Kc=\frac {{[C]_{eq}}^c{[D]_{eq}}^d}{{[A]_{eq}}^a{[B]_{eq}}^b}$$
Vamos a desglosarlo.
En primer lugar, los corchetes indican concentración. Así que [A] significa simplemente la concentración de A en el equilibrio, en mol·L-1 . ¿Y la pequeña letra superíndice a la derecha de [A]? Procede de la relación molar. Significa que tomamos la concentración de A y la elevamos a la potencia del número de moles de A, que se da en la ecuación de reacción.
Observa que en la ecuación, las concentraciones de los productos están en la parte superior de la fracción, y las concentraciones de los reactantes están en la parte inferior. También podemos simplificar la ecuación eliminando el pequeño subíndice eq de cada concentración; no importa, siempre que recuerdes que necesitas la concentración en el equilibrio.
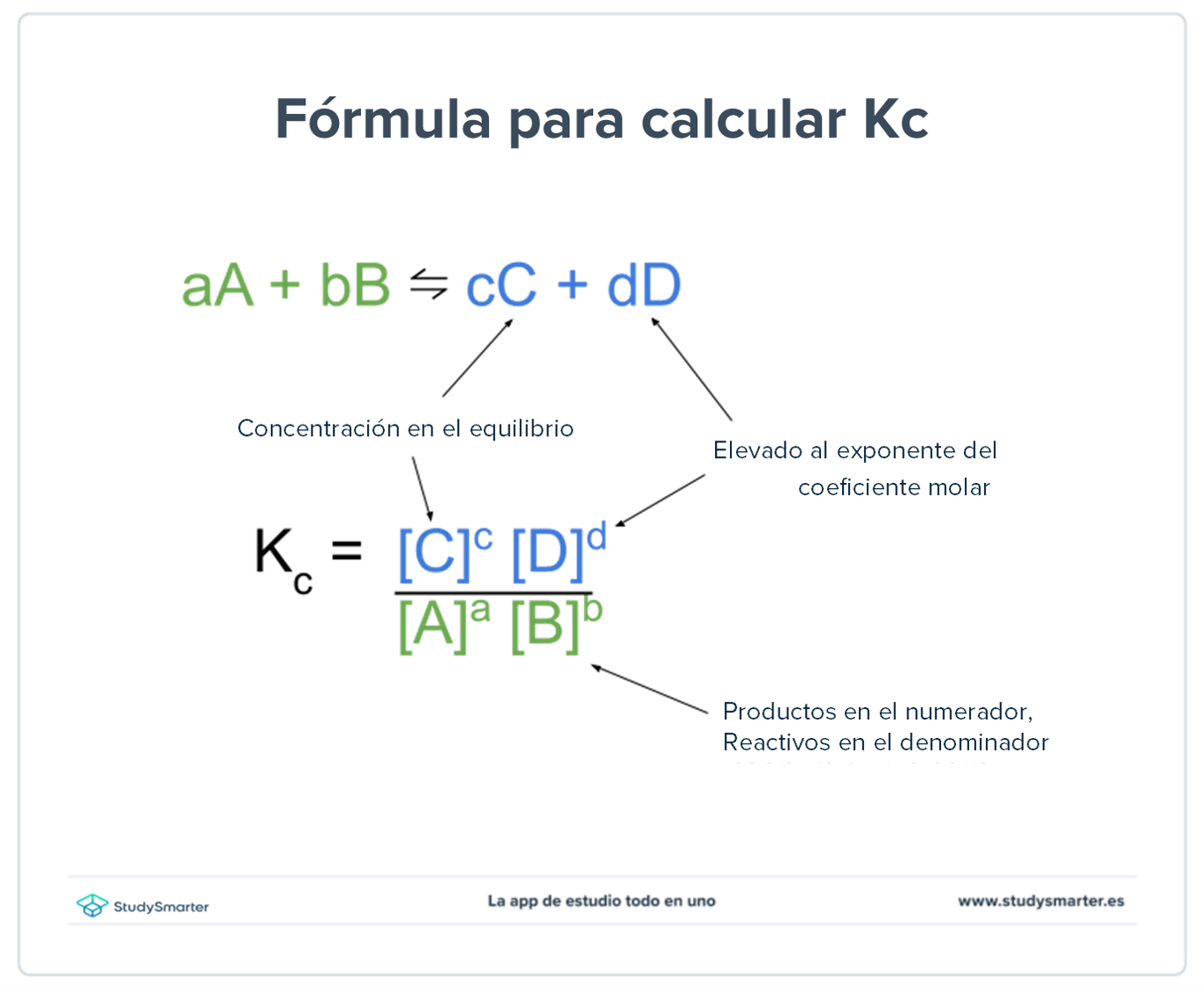
Fig. 1: Fórmula para calcular Kc
He aquí un ejemplo.
$$2SO_{2(g)}+O_{2(g)}\rightleftharpoons 2SO_{3(g)}$$
¿Cuál sería la constante de equilibrio de esta reacción?
- Toma las concentraciones de equilibrio de los productos.
- Súbelas a la potencia de la relación molar dada en la ecuación.
- Divídelas por las concentraciones de equilibrio de los reactantes, elevadas a la potencia de la relación molar dada en la ecuación.
En este caso, nuestro único producto es el SO3. Tenemos 2 moles del mismo en la ecuación. Nuestros reactantes son SO2 y O2. Tenemos 2 moles del primero y 1 mol del segundo. Por tanto, nuestra ecuación para Kc debería tener este aspecto:
$$Kc=\frac {[SO_3]^2}{[SO_2]^2[O_2]}$$
En este ejemplo, la reacción es un ejemplo de equilibrio homogéneo: todas las especies están en el mismo estado. ¿Cómo calculamos el Kc para equilibrios heterogéneos?
Bueno, el Kc implica concentración. En realidad, no puedes medir la concentración de un sólido. Si tenemos un equilibrio en el que intervienen gases y un sólido, por ejemplo, simplemente ignoramos el sólido en la ecuación para Kc.

Fig. 2: Fórmula para calcular Kc en un equilibrio heterogéneo
Unidades de la constante de equilibrio para Kc
Las unidades de Kc pueden variar de un cálculo a otro. Todo depende de la reacción con la que estés trabajando. Necesitarás saber cómo calcular estas unidades, paso a paso.
- Toma la ecuación para Kc.
- Sustituye la concentración de cada especie por las unidades en las que se mide la concentración.
- Anula las unidades de la parte superior e inferior de la ecuación hasta que solo te quede un término.
Tomemos nuestro ejemplo anterior. Todas las concentraciones se miden en mol dm-3, por lo que la ecuación tiene ahora este aspecto:
$$Unidades=\frac {(mol\cdot L^{-1})^2}{(mol \cdot L^{-1})^2(mol \cdot L^{-1})}$$
Si los anulamos, acabamos con esto:
$$Unidades=\frac {1}{(mol \cdot L^{-1})}=mol^{-1}\cdot L$$
A veces Kc no tiene unidades. Mira esta ecuación para una reacción de esterificación reversible:
$$CH_3COOH_{(aq)}+CH_3CH_2OH_{(aq)}\rightleftharpoons CH_3COOCH_2CH_{3(aq)}+H_2O_{(l)}$$
Si encontramos una ecuación para Kc, obtenemos lo siguiente:
$$Kc=\frac {[CH_3COOCH_2CH_3][H_2O]}{[CH_3COOH][CH_3CH_2OH]}$$
Cuando ponemos las unidades, obtenemos (mol dm-3)(mol dm-3) arriba, y (mol dm-3)(mol dm-3) abajo. Esto se anula para dar 1, por lo que no hay unidades:
$$Unidades=\frac {(mol \cdot L^{-1})(mol \cdot L^{-1})}{(mol \cdot L^{-1})(mol \cdot L^{-1})}$$
Cálculo de la constante de equilibrio Kc
En las preguntas de los exámenes, normalmente se te dan las concentraciones iniciales de los reactantes. Se te indica algún aspecto de la solución de equilibrio y tienes que calcular las concentraciones de todos los reactivos y productos en el equilibrio. Entonces puedes calcular Kc.
En un recipiente hermético de 600 mL de volumen, 0,500 mol de H2 y 0,600 mol de Cl2 reaccionan formando un equilibrio con la siguiente ecuación:
$$H_{2(g)}+Cl_{2(g)}\rightleftharpoons 2HCl_{(g)}$$
En el equilibrio, hay 0,400 mol de HCl presentes en el recipiente. Halla un valor para Kc. Incluye las unidades en tu respuesta.
En primer lugar, vamos a hacer una tabla. Vamos a utilizar la información que nos han dado en la pregunta para rellenar esta tabla. Para cada especie, pondremos el número de moles al inicio de la reacción, el cambio en el número de moles y el número de moles en el equilibrio. También querrás una fila para la concentración en el equilibrio.
| \(H_2\) | \(Cl_2\) | \(HCl\) |
| Número de moles al inicio | | | |
| Cambio en el número de moles | | | |
| Número de moles en el equilibrio | | | |
| Concentración en el equilibrio | | | |
Para empezar, escribe el número de moles de todas las especies implicadas al inicio de la reacción. La pregunta nos los daba. La pregunta no mencionaba ningún mol de ácido clorhídrico, así que podemos suponer que no había ninguno.
| \(H_2\) | \(Cl_2\) | \(HCl\) |
| Número de moles al inicio | 0,500 | 0,600 | 0,000 |
| Cambio en el número de moles | | | |
| Número de moles en el equilibrio | | | |
| Concentración en el equilibrio | | | |
La pregunta nos dice que en el equilibrio hay 0,4 moles de HCl presentes. Escribe este valor en la tabla.
| \(H_2\) | \(Cl_2\) | \(HCl\) |
| Número de moles al inicio | 0,500 | 0,600 | 0,000 |
| Cambio en el número de moles | | | |
| Número de moles en el equilibrio | | | 0,400 |
| Concentración en el equilibrio | | | |
Ahora podemos calcular el cambio en los moles de HCl. Al principio de la reacción, no había nada de HCl. En el equilibrio, hay 0,400 moles. Esto supone un cambio de +0,400.
Si echamos un vistazo a la ecuación de la reacción de equilibrio, veremos que por cada dos moles de HCl formados, se consumen un mol de H2 y un mol de Cl2. La relación molar es, por tanto, 1:1:2. Para averiguar el número de moles de H2 y Cl2 consumidos en la reacción, divide el número de moles de HCl formados (el cambio en moles) por 2.
$$\frac {0,400}{2}=0,200$$
Por tanto, en la reacción se consumen 0,200 moles de H2 y 0,200 moles de Cl2, para formar 0,400 moles de HCl. El cambio en moles de estas dos especies es por tanto -0,200.
| \(H_2\) | \(Cl_2\) | \(HCl\) |
| Número de moles al inicio | 0,500 | 0,600 | 0,000 |
| Cambio en el número de moles | -0,200 | -0,200 | +0,400 |
| Número de moles en el equilibrio | | | 0,400 |
| Concentración en el equilibrio | | | |
Una vez conocido el cambio en el número de moles de cada especie, podemos calcular el número de moles en el equilibrio. Para ello, suma el cambio en el número de moles al número de moles al inicio de la reacción.
Para el H2: \(0,500 + (-0,200)=0,300\)
Para el Cl2: \(0,500 + (-0,200)=0,300\)
Escríbelos en tu tabla.
Recuerda que Kc utiliza la concentración de equilibrio, no el número de moles. Pero como conocemos el volumen del recipiente, podemos calcularlo fácilmente. Acuérdate de poner el volumen en L. En este caso, 600 mL = 0,600 L.
$$[X]=\frac {moles\ X}{volumen\ (L)}$$
Para H2: \(\frac {0,300\ moles\ H_2}{0,600\ L}=0,500 mol \cdot L^{-1}\)
Para Cl2: \(\frac {0,400\ moles\ H_2}{0,600\ L}=0,667 mol \cdot L^{-1}\)
Para HCl: \(\frac {0,400\ moles\ H_2}{0,600\ L}=0,667 mol \cdot L^{-1}\)
| \(H_2\) | \(Cl_2\) | \(HCl\) |
| Número de moles al inicio | 0,500 | 0,600 | 0,000 |
| Cambio en el número de moles | -0,200 | -0,200 | +0,400 |
| Número de moles en el equilibrio | 0,300 | 0,400 | 0,400 |
| Concentración en el equilibrio | 0,500 | 0,667 | 0,667 |
Ahora podemos mirar la expresión para Kc, la cual se verá así:
$$\frac {[HCl]^2}{[Cl_2][H_2]}$$
A continuación podemos sustituir los valores que tenemos para la concentración en el equilibrio en la ecuación para Kc:
$$\frac {(0,667)^2}{(0,667)(0,500)}=1,33$$
El paso final es encontrar las unidades de Kc. Para ello, introduce las unidades de cada una de las concentraciones en la ecuación para Kc y cancélalas. En este caso, se cancelan completamente para dar 1. Aquí, Kc no tiene unidades:
$$\frac {(mol \cdot L^{-1})^2}{(mol\cdot L^{-1})(mol\cdot L^{-1})}=\frac {(mol\cdot L^{-1})^2}{(mol\cdot L^{-1})^2}=1$$
Asi que, nuestra respuesta final es 1,33.
Aquí tienes otra pregunta:
5,0 moles de O2 y 5,0 moles de SO2 alcanzan el equilibrio dinámico en un recipiente de volumen 12 L. El equilibrio contiene 3,0 moles de SO3. Halla Kc e indica sus unidades. La siguiente ecuación puede ayudarte:
$$O_2+2SO_2\rightleftharpoons 2SO_3$$
Escribamos nuestra tabla, como antes:
| \(O_2\) | \(SO_2\) | \(SO_3\) |
| Número de moles al inicio | 5,0 | 5,0 | 0,0 |
| Cambio en el número de moles | | | |
| Número de moles en el equilibrio | | | |
| Concentración en el equilibrio | | | |
En el equilibrio, tenemos 3 moles de SO3. Por tanto, el cambio de moles es +3. Como nuestra relación molar es 1:2:2, el cambio en moles de O2 debe ser -0,15 y el cambio en moles de SO2 debe ser -0,3. Ahora podemos calcular el número de moles de cada especie en equilibrio y sus concentraciones, utilizando el volumen dado de 12 L:
$$\begin {align} n_{O_2}&=5-1,5=3,5\ moles \\ [O_2]&=\frac {3,5\ moles}{12\ L}=0,29\ mol\cdot L^{-1} \end {align}$$
$$\begin {align} n_{SO_2}&=5-3=2\ moles \\ [SO_2]&=\frac {2\ moles}{12\ L}=0,17\ mol\cdot L^{-1} \end {align}$$
$$\begin {align} n_{SO_3}&=0,0+3=3\ moles \\ [SO_3]&=\frac {3\ moles}{12\ L}=0,25\ mol\cdot L^{-1} \end {align}$$
Tu tabla debe tener este aspecto:
| \(O_2\) | \(SO_2\) | \(SO_3\) |
| Número de moles al inicio | 5,0 | 5,0 | 0,0 |
| Cambio en el número de moles | -1,5 | -3,0 | +3,0 |
| Número de moles en el equilibrio | 3,5 | 2,0 | 3,0 |
| Concentración en el equilibrio | 0,29 | 0,17 | 0,25 |
La ecuación para Kc es la siguiente:
$$Kc=\frac {[SO_3]^2}{[O_2][SO_2]^2}$$
Introduciendo la concentración tienes:
$$Kc=\frac {(0,25)^2}{(0,29)(0,17)^2}=7,7$$
Para hallar las unidades, debes cancelar las unidades de concentración:
$$\frac {(mol \cdot L^{-1})^2}{(mol\cdot L^{-1})(mol\cdot L^{-1})^2}=\frac {1}{(mol\cdot L^{-1})}=mol^{-1}\cdot L$$
La respuesta final será entonces 7,7 mol-1 L.
Si tienes problemas con el cálculo de Kc puedes usar el siguiente diagrama de flujo que debería simplificar el proceso para ti.
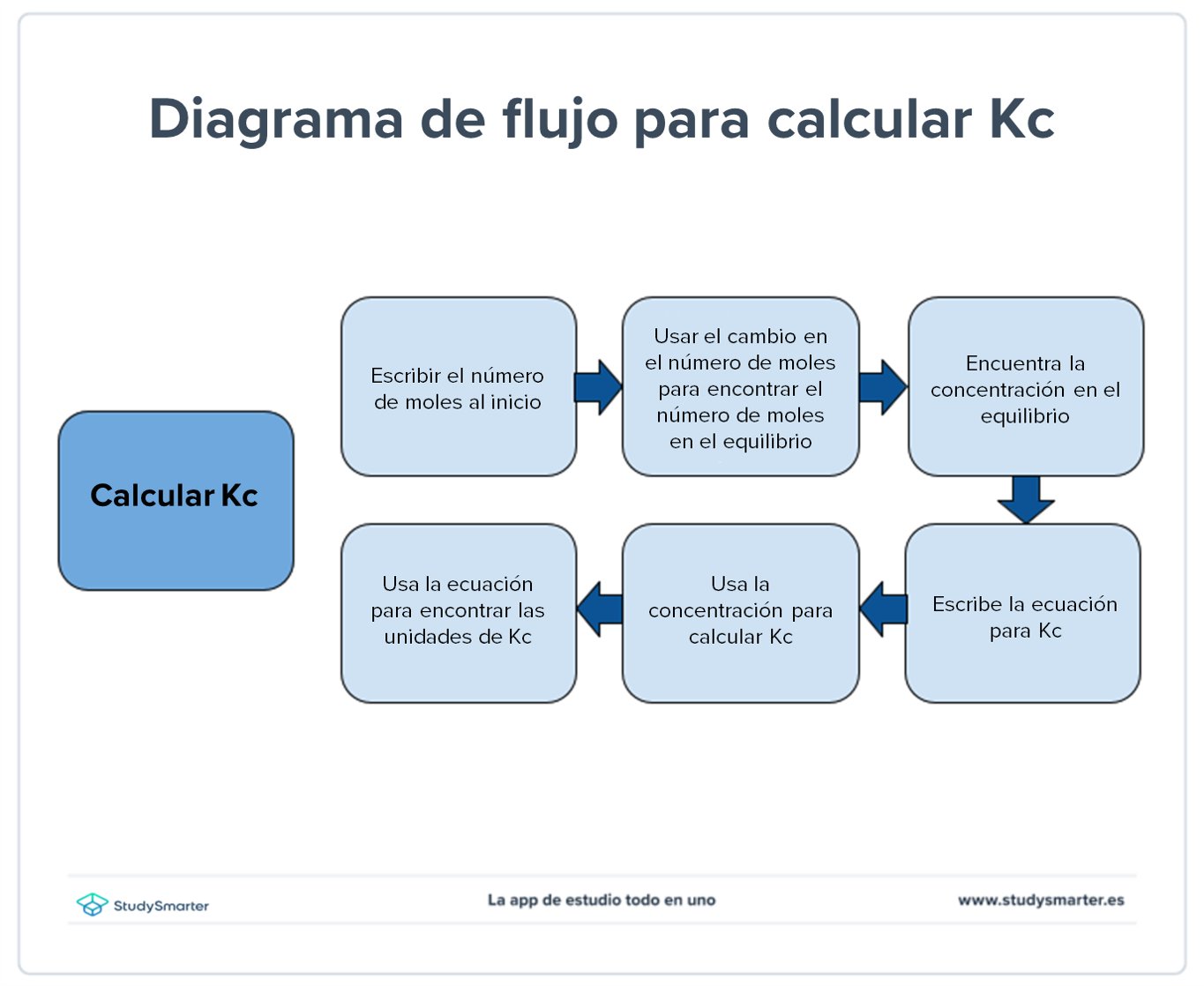
Fig. 3: Diagrama de flujo para calcular Kc.
Trabajando a partir de Kc
A veces, te darán la constante Kc de una reacción y tendrás que calcular el número de moles de cada especie en el equilibrio. Esto es un poco más complicado e implica resolver una ecuación cuadrática. Veamos juntos un ejemplo.
1 mol de etanoato de etilo y 5 moles de agua reaccionan formando un equilibrio dinámico en un recipiente con un volumen de 1 L. El Kc para esta reacción es 10,0. Halla el número de moles de cada sustancia en equilibrio, ayudándote de la siguiente ecuación:
$$CH_3COOCH_2CH_{3(g)}+H_2O_{(g)}\rightleftharpoons CH_3COOH_{(g)}+CH_3CH_2OH_{(g)}$$
Empecemos por escribir en una tabla los valores que sí conocemos. Sabemos que al principio tenemos 1 mol de etanoato de etilo y 5 moles de agua. Para formar un equilibrio, parte del etanoato de etilo y del agua reaccionarán para formar etanol y ácido etanoico.
También sabemos que la relación molar es 1:1:1:1. Por cada mol de etanoato de etilo que se consuma, se consumirá también un mol de agua, formándose un mol de etanol y un mol de ácido etanoico. Sin embargo, no sabemos qué cantidad de etanoato de etilo y de agua reaccionará. Podemos mostrar este valor desconocido utilizando el símbolo x.
Empezamos con 1 mol de etanoato de etilo. Si reaccionan x moles de este, entonces nuestra mezcla de equilibrio contendrá 1 - x moles de etanoato de etilo. Del mismo modo, empezamos con 5 moles de agua. Como la relación molar es 1:1:1:1, también reaccionarán x moles de agua, por lo que el número de moles de agua en el equilibrio es 5 - x.
¿Cuánto etanol y ácido etanoico tenemos en el equilibrio? Empezamos con 0 moles de cada uno, y sabemos por la relación molar que produciremos x moles de cada uno. Esto significa que en el equilibrio tenemos exactamente x moles de etanol y x moles de ácido etanoico.
Si haces una tabla mostrando todos los valores, debería tener este aspecto:
| \(CH_3COOCH_2CH_3\) | \(H_2O\) | \(CH_3COOH\) | \(CH_2CH_3\) |
| Número de moles al inicio | 1,0 | 5,0 | 0,0 | 0,0 |
| Cambio en el número de moles | -x | -x | +x | +x |
| Número de moles en el equilibrio | 1,0 - x | 5,0 - x | x | x |
| Concentración en el equilibrio | | | | |
Para hallar la concentración de cada especie en equilibrio, dividimos el número de moles de cada especie en equilibrio por el volumen del recipiente. En este caso, el volumen es 1 L. Cualquier cosa dividida por 1 da sí mismo, por lo que aquí la concentración en equilibrio es la misma que el número de moles en equilibrio.
| \(CH_3COOCH_2CH_3\) | \(H_2O\) | \(CH_3COOH\) | \(CH_2CH_3\) |
| Número de moles al inicio | 1,0 | 5,0 | 0,0 | 0,0 |
| Cambio en el número de moles | -x | -x | +x | +x |
| Número de moles en el equilibrio | 1,0 - x | 5,0 - x | x | x |
| Concentración en el equilibrio | 1,0 - x | 5,0 - x | x | x |
Ahora, escribamos una ecuación para Kc:
$$Kc=\frac {[CH_3COOH][CH_2CH_3]}{[CH_3COOCH_2CH_3][H_2O]}$$
Podemos introducir nuestros valores de concentración. En la pregunta, también nos dieron un valor para Kc, que también podemos introducir. Esto significa que la única incógnita es x:
$$10,0=\frac {(x)(x)}{(1-x)(5-x)}$$
Multiplica ambos lados de la ecuación por (1-x) (5-x):
$$10,0\times (1-x)(5-x)=(x)(x)$$
Expande los paréntesis para hacer una ecuación cuadrática en términos de x y reordénala para que sea igual a 0:
$$10x^2-60x+50=x^2$$
$$9x^2-60x+50=0$$
Ahora puedes resolverlo con la calculadora. Deberías obtener dos valores para x: 5,69 y 0,976. ¿Cómo sabes cuál es el correcto?
Bien, recuerda que x es igual al número de moles de etanoato de etilo y agua que reaccionaron para formar un equilibrio dinámico. Solo empezamos con 1 mol de etanoato de etilo. Si reaccionaran 5,69 moles de etanoato de etilo, nos quedaríamos con -4,69 moles, lo cual no es posible, ¡no se puede tener un número negativo de moles! Por lo tanto, x debe ser igual a 0,976.
Para terminar esta pregunta, ahora podemos hallar el número de moles de cada especie en el equilibrio:
$$n_{CH_3COOCH_2CH_3}=1-x=1-0,976=0,024\ moles$$
$$n_{H_2O}=5-x=5-0,976=4,024\ moles$$
$$n_{CH_3COOH}=x=0,976\ moles$$
$$n_{CH_3COOH}=x=0,976\ moles$$
Habrás observado que solo hemos calculado Kc para sistemas homogéneos. Se trata de sistemas en los que todos los productos y reactivos están en el mismo estado, por ejemplo, todos líquidos o todos gases. Sin embargo, también podemos calcular el Kc para mezclas heterogéneas si algunas de las especies son sólidos. En estos casos, la ecuación para el Kc simplemente ignora los sólidos.
Tomemos el siguiente ejemplo:
$$Cu_{(s)}+2Ag^{+}_{(aq)}\rightleftharpoons Cu^{+2}_{(aq)}+2Ag_{(s)}$$
Para esta reacción, \(Kc=\frac {[Cu^{+2}]}{[Ag^+]^2}\). Ignoramos las concentraciones de cobre y plata porque son sólidos.
Magnitud de la constante de equilibrio Kc
A partir de la magnitud de Kc, podemos deducir algunas cosas importantes sobre la reacción a esa temperatura específica:
- Si Kc es menor que 1, entonces el denominador de la ecuación para Kc debe ser mayor que el numerador. Por lo tanto, tenemos una mayor concentración de reactivos que de productos en el equilibrio. Esto significa que la posición del equilibrio se encuentra a la izquierda y predomina la reacción hacia atrás.
- Si Kc es igual a 1, entonces el numerador y el denominador de la ecuación para Kc deben ser iguales. Por tanto, tenemos concentraciones iguales de reactivos y productos en el equilibrio. Esto significa que la posición del equilibrio se encuentra en el centro.
- Si Kc es mayor que 1, entonces el numerador de la ecuación para Kc debe ser mayor que el denominador. Por lo tanto, tenemos una mayor concentración de productos que de reactivos en el equilibrio. Esto significa que la posición del equilibrio está a la derecha y que predomina la reacción de avance.
Factores que afectan a la constante de equilibrio Kc
Por último, echemos un vistazo a los factores que afectan al Kc. En realidad es bastante fácil de recordar: solo la temperatura afecta al Kc. La presión, la concentración y la presencia de un catalizador no tienen ningún efecto sobre el Kc.
Tomemos este ejemplo de reacción:
$$N_{2(g)}+3H_{2(g)}\rightleftharpoons 2NH_{3(g)} \qquad \Delta H=-92\ kJ\cdot mol^{-1}$$
Si disminuimos la temperatura, la reacción exotérmica de avance se verá favorecida y, por tanto, el equilibrio se desplazará hacia la derecha. Se produce más producto, lo que significa que aumenta su concentración y, por tanto, también aumenta el valor de Kc. Aumentar la temperatura favorece la reacción hacia atrás y disminuye el valor de Kc.
Aplicaciones de la constante de equilibrio Kc
La constante de equilibrio Kc es útil porque nos permite manipular las condiciones de un equilibrio para influir en el rendimiento. Un ejemplo es el proceso de Haber, utilizado para fabricar amoníaco. De hecho, esta es la reacción que hemos explorado anteriormente:
$$N_{2(g)}+3H_{2(g)}\rightleftharpoons 2NH_{3(g)} \qquad \Delta H=-92\ kJ\cdot mol^{-1}$$
Sabemos que, a una temperatura determinada, Kc es siempre constante (su nombre nos delata un poco). Esto significa que en el equilibrio siempre habrá la misma proporción de productos y reactivos en la mezcla. En este caso, nuestro producto es el amoníaco y nuestros reactantes son el nitrógeno y el hidrógeno.
Supongamos que queremos maximizar nuestro rendimiento de amoníaco. Para ello, podemos añadir muchos gases de nitrógeno e hidrógeno a la mezcla. Esto aumenta sus concentraciones. Sin embargo, Kc dice que la relación entre nitrógeno e hidrógeno y amoníaco no puede cambiar, por lo que parte del nitrógeno y el hidrógeno se convertirán en amoníaco para que las concentraciones vuelvan a sus niveles de equilibrio. La reacción hacia delante se ve favorecida y nuestro rendimiento de amoníaco aumenta. Este es solo un ejemplo de aplicación de Kc.
La constante de equilibrio Kp - Key takeaways
- Kc es un tipo de constante de equilibrio que relaciona la concentración de reactivo y la concentración de producto en una mezcla en equilibrio.
- Cuanto mayor sea el valor de Kc, mayor será la proporción de producto en relación con el reactante en el equilibrio.
- Para la reacción general aA + bB ⇌ cC + dD, \(Kc=\frac {[C]^c[D]^d}{[A]^a[B]^b}\)
- Para hallar las unidades de Kc, sustituyes las unidades de concentración en la ecuación para Kc y las cancelas.
- Para calcular Kc, tienes que calcular el número de moles de cada especie en equilibrio y su concentración en equilibrio.
- La magnitud de Kc nos habla de la posición de equilibrio.
- El valor de Kc se ve afectado por la temperatura, pero no por la concentración, la presión y la presencia de un catalizador.
- Las constantes de equilibrio nos permiten manipular las condiciones de un equilibrio para aumentar su rendimiento.










