En este artículo veremos qué son los polímeros, cómo se forman y cuáles son sus tipos más comunes.
Algunos ejemplos de polímeros son las proteínas, el ADN y los plásticos, como el policloruro de vinilo (PVC) y el poliestireno.
Nos centraremos aquí en estos plásticos —incluyendo las poliamidas, los poliésteres y los polímeros hechos de alquenos— y en las reacciones que los forman, que se conocen colectivamente como reacciones de polimerización.
- En primer lugar, repasaremos la definición de polímeros y monómeros.
- Después, profundizaremos en los mecanismos de polimerización.
- Veremos algunos ejemplos comunes de polímeros.
- Por último, trataremos brevemente los polímeros termoestables.
¿Qué son los polímeros?
Los polímeros son compuestos orgánicos formados por largas cadenas de unidades repetitivas llamadas monómeros.
Los monómeros suelen ser pequeñas moléculas que tienen la capacidad (o propensión) de formar polímeros debido a su disposición estructural y a sus propiedades químicas. Por lo que los polímeros están formados por monómeros que constan del mismo bloque de construcción.
La definición de polímeros viene de "poli", que significa muchos. Esto se debe a que los polímeros están formados por muchas unidades de monómeros.
La polimerización es la reacción que produce los polímeros, incluyendo la reacción de dos monómeros para formar un dímero.
Para producir cadenas más largas de polímeros y garantizar el crecimiento de la cadena de polímeros, se pueden añadir monómeros posteriores,, mediante el mismo mecanismo de polimerización; para ello, los monómeros tienen que ser de la misma naturaleza química.
Los polímeros pueden proceder de dos monómeros únicos, homopolímeros o de un monómero que contenga dos grupos funcionales diferentes: copolímeros. Los monómeros que contengan dos funcionales diferentes, dependiendo de las estructuras de los monómeros o las condiciones, puede formar: copolímeros alternados, en bloque o al azar.
Monómero y polímero
La siguiente tabla muestra algunos ejemplos de monómeros y sus polímeros:
| Nombre del monómero | Estructura del monómero | Nombre del polímero | Estructura de polímero |
| Propeno | | Polipropileno | |
| 2-metilpropenoato de metilo | | Poli(metil-2-metilpropenoato), o PMMA | |
| Fenileteno | | Polifenileteno también conocido como el poliestireno | |
Tabla 1. Una tabla que muestra diferentes monómeros y sus polímeros.
Tipos de polimerización
Se puede clasificar los polímeros según su polimerización, pues se produce mediante dos mecanismos principales: la polimerización por adición y la polimerización por condensación. Estas dependen de los grupos funcionales del monómero o monómeros involucrados.
- La polimerización por adición se forma cuando se rompe un doble enlace carbono-carbono, sin dar lugar a ningún subproducto.
- La polimerización por condensación se da cuando reaccionan las moléculas con grupos funcionales diferentes; tienen como subproducto una molécula pequeña, como el agua.
Polimerización por adición
La polimerización por adición es un mecanismo de polimerización en el cual un compuesto orgánico, que contiene un doble enlace, reacciona mediante una serie de etapas y genera un polímero del monómero de partida.
Como ya has visto en mecanismos de reacción, las reacciones en química orgánica se basan en el movimiento de electrones. Los alquenos pueden someterse a la polimerización por adición, para formar polímeros de cadenas largas de hidrocarburos. El doble enlace tiene un enlace, cuyos electrones tienen la capacidad de formar un enlace con otra molécula, lo que crea una cadena carbonada. Los monómeros utilizados pueden ser todos del mismo alqueno o de varios tipos diferentes. Esto se muestra a continuación, con el ejemplo del eteno:
 Fig. 2- Polimerización por adición con eteno.
Fig. 2- Polimerización por adición con eteno.
En la polimerización por adición no se producen subproductos.
Representación de los polímeros de adición
La polimerización por adición puede representarse mediante una ecuación de polimerización (Ver más abajo).
- -R representa cualquier grupo alquilo o arilo variable.
- n representa el número de monómeros de alqueno utilizados, que suele ser muy grande.
Un grupo arilo se refiere a un sustituyente, derivado de un hidrocarburo aromático.
 Fig. 3- La polimerización de un compuesto químico
Fig. 3- La polimerización de un compuesto químico
Esto se llama ecuación de polimerización.
Nomenclatura
Los polímeros de adición se nombran utilizando el prefijo poli- y el nombre de su monómero alqueno. Por ejemplo, el cloroeteno se polimeriza para formar policloroeteno. Sin embargo, muchos de estos polímeros tienen diferentes nombres comerciales, y el policloroeteno se conoce como cloruro de polivinilo o PVC.
Cómo deducir el monómero, según el polímero
Cuando te pidan que encuentres la unidad de repetición de un determinado polímero de adición, debes recordar que cada monómero se basa en un doble enlace C=C. Por lo tanto, cada par de carbonos en el esqueleto C-C del polímero pertenecerá a un monómero diferente.
Los monómeros también se pueden trabajar identificando el patrón de repetición del polímero, como en el ejemplo siguiente:
 Fig. 4- Del polímero al monómero.
Fig. 4- Del polímero al monómero.
La polimerización por radicales libres es un tipo de polimerización por adición, en la que un radical libre reacciona con el monómero (mediante unas reacciones consecutivas) para formar un polímero.
Un radical libre es una especie con un electrón de la capa externa desapareado.
Se forma el radical libre por calentamiento o radiación. Esto causa una ruptura homolítica del enlace, lo que significa que cada una de las dos nuevas moléculas aceptan un electrón y crean dos radicales libres. Esta etapa se denomina iniciación.
A continuación, el radical reacciona con un monómero, formando un radical más grande, llamado propagación. Esto se muestra en la siguiente ecuación —donde R es un radical libre y M es un monómero—:
Luego, el radical libre formado reacciona con otra molécula del monómero:
Posteriormente, reaccionan hasta la etapa de la terminación, que implica que dos radicales reaccionan juntos para formar un compuesto estable:
La polimerización de radicales libres puede representarse mediante la siguiente ecuación general:
Polimerización por condensación
La polimerización por condensación es una reacción en la que los monómeros se unen para formar un polímero más corto que los polímeros formados por polimerización por adición, liberando una pequeña molécula en el proceso.
A continuación, veremos unos ejemplos y reacciones de condensación:
Polímeros: ejemplos
Algunos ejemplos de polímeros de condensación son
Poliamidas
Las poliamidas se forman en la reacción entre una amina y un ácido carboxílico. Como cada monómero debe tener dos grupos funcionales para formar un polímero, los monómeros suelen ser diaminoalcanos y ácidos dicarboxílicos.
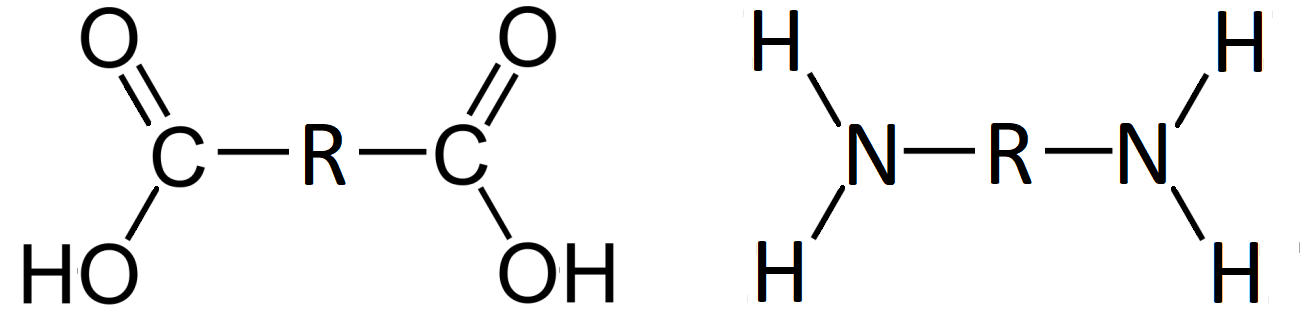
Fig. 5: un ácido dicarboxílico —a la izquierda— y una diamina —a la derecha—.
El subproducto que se genera es agua, formando un enlace covalente entre el carbono del grupo carboxílico y el nitrógeno del grupo amina, para dar lugar a un grupo funcional amida -NCO-.
Esto puede representarse mediante la siguiente ecuación:
 Fig. 6- Una reacción de condensación entre una diamina y un ácido dicarboxílico forma una poliamida
Fig. 6- Una reacción de condensación entre una diamina y un ácido dicarboxílico forma una poliamida
El Nylon-6,6 se fabrica a partir de 1,6-diaminohexano y ácido hexano-1,6-dicarboxílico:
 Fig. 7- Nylon-6,6
Fig. 7- Nylon-6,6
Poliésteres
Los poliésteres se forman a partir de alcoholes y ácidos carboxílicos. Los monómeros a menudo son dioles y ácidos dicarboxílicos.
 Fig. 8- Un diol, a la izquierda, y un ácido dicarboxílico, a la derecha
Fig. 8- Un diol, a la izquierda, y un ácido dicarboxílico, a la derecha
De nuevo, el subproducto es agua, con lo que el grupo funcional éster -COO- se repite en toda la molécula. La ecuación general se muestra a continuación:
 Fig. 9- Una reacción de condensación entre un diol y un ácido dicarboxílico forma un poliéster.
Fig. 9- Una reacción de condensación entre un diol y un ácido dicarboxílico forma un poliéster.
Para más información sobre los alcoholes, las aminas o los ácidos carboxílicos, consulta Alcoholes, Aminas y Ácidos Carboxílicos y Ésteres, respectivamente.
Cómo deducir el monómero a partir del polímero
Para identificar los monómeros utilizados de una cadena polimérica, puede ser útil localizar el grupo funcional -COO- o -NCO- que se repite. A continuación, puedes dividir la molécula en sus unidades repetitivas.
Por ejemplo, este polímero está formado por 1,2-etanodiol y ácido butano-1,4-dioico:
 Fig. 10- Síntesis de tereftalato de polietileno
Fig. 10- Síntesis de tereftalato de polietileno
A veces, solo se necesita un monómero para una reacción de condensación. Esto ocurre si la molécula contiene dos grupos funcionales adecuados diferentes; por ejemplo, las proteínas.
Las proteínas son un tipo de polímero que también se forma en una reacción de condensación. Las proteínas están formadas por largas cadenas de aminoácidos, cada una de las cuales contiene un grupo amino y un grupo carboxilo. Estos reaccionan juntos para formar una poliamida:
 Fig. 11- Los amino ácidos forman las proteínas mediante una reacción de condesación
Fig. 11- Los amino ácidos forman las proteínas mediante una reacción de condesación
Similitudes y diferencias
La siguiente tabla muestra las similitudes y diferencias entre la polimerización por adición y por condensación:
| Nombre | Adición | Condesación |
| Número de grupos funcionales | 1 | 2 |
| Ejemplos de grupos funcionales | C=C | -COOH, -OH, -NH2 |
| Nombre del producto principal | Poli (nombre de alqueno) | eg. Poliester (poli + grupo funcional formado) |
| Subproductos | Ninguno | Si, y muchas veces es agua |
Tabla 2: Comparación de la polimerización por adición y por condensación.
Polímeros - Puntos clave
- Los polímeros son grandes moléculas formadas por unidades repetitivas llamadas monómeros.
- Los polímeros de adición están formados por monómeros de alqueno con un doble enlace C=C.
- Se pueden formar por polimerización de adición o de condensación.
- Los polímeros de condensación están formados por monómeros con dos grupos funcionales diferentes, como los ácidos carboxílicos y los alcoholes.
- La polimerización por adición es un mecanismo de polimerización en el cual un compuesto orgánico, que contiene un doble enlace, reacciona mediante una serie de etapas para generar un polímero del monómero de partida.

















