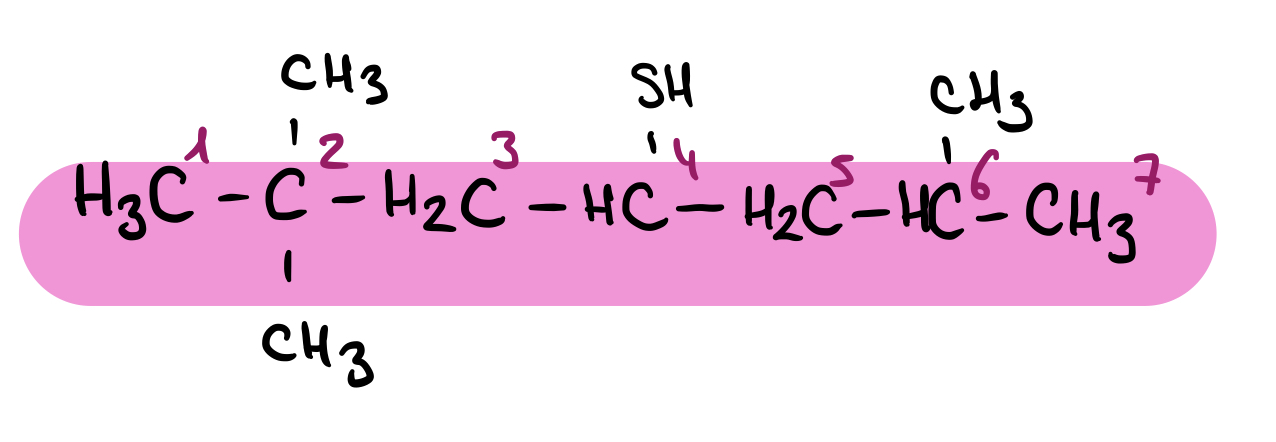Lily Hulatt es una especialista en contenido digital con más de tres años de experiencia en estrategia de contenido y diseño curricular. Obtuvo su doctorado en Literatura Inglesa en la Universidad de Durham en 2022, enseñó en el Departamento de Estudios Ingleses de la Universidad de Durham y ha contribuido a varias publicaciones. Lily se especializa en Literatura Inglesa, Lengua Inglesa, Historia y Filosofía.
Conoce a Lily




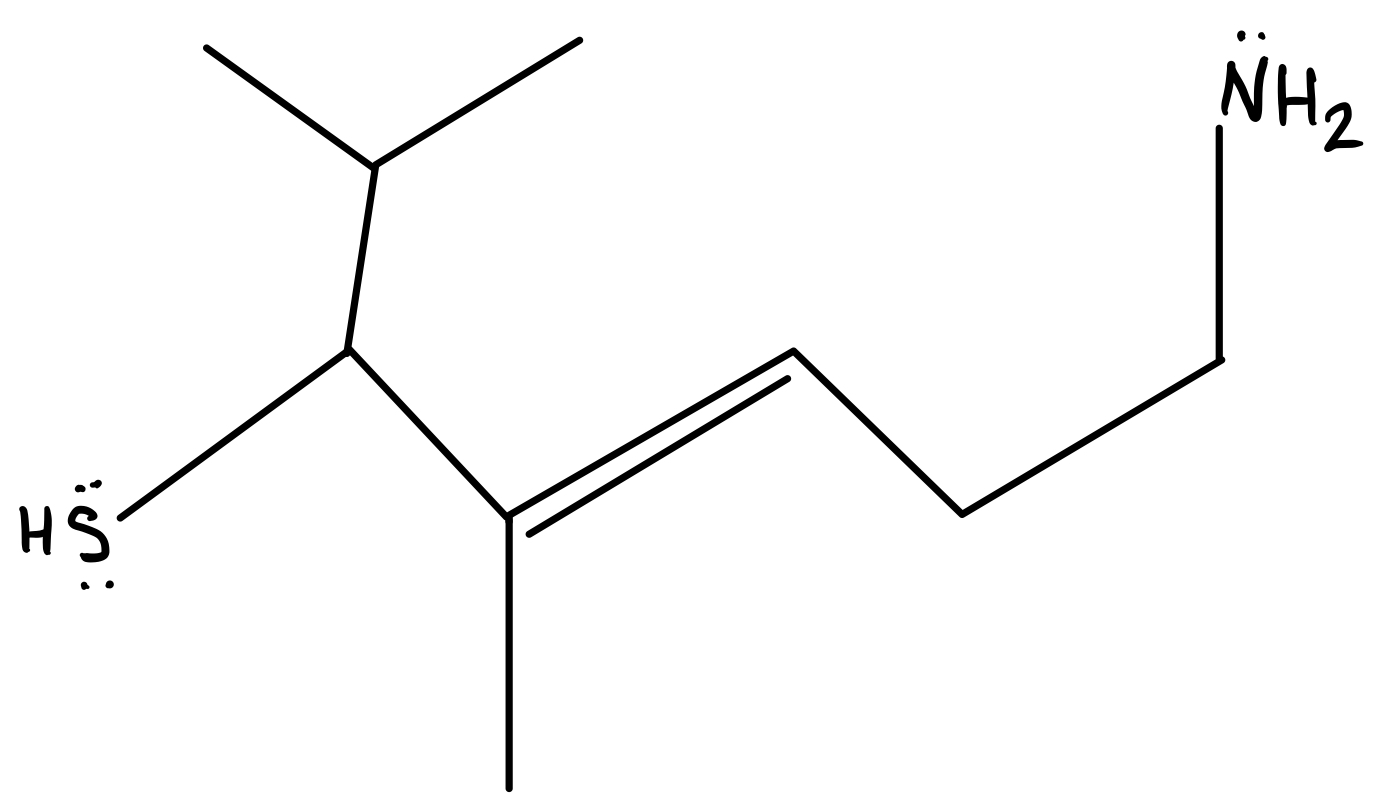
 Figura 5: Observa que la cadena más larga de carbonos, en la que se encuentra el grupo funcional prioritario, tiene siete carbonos.
Figura 5: Observa que la cadena más larga de carbonos, en la que se encuentra el grupo funcional prioritario, tiene siete carbonos.